 |
|
 |
|
farmaci
18 Luglio 2025L’Agenzia Italiana del Farmaco (Aifa) ha adottato le Istruzioni applicative datate 17 luglio 2025 in cui fornisce un quadro operativo per l’implementazione del nuovo sistema anticontraffazione dei medicinali previsto dal decreto legislativo 6 febbraio 2025, n. 10
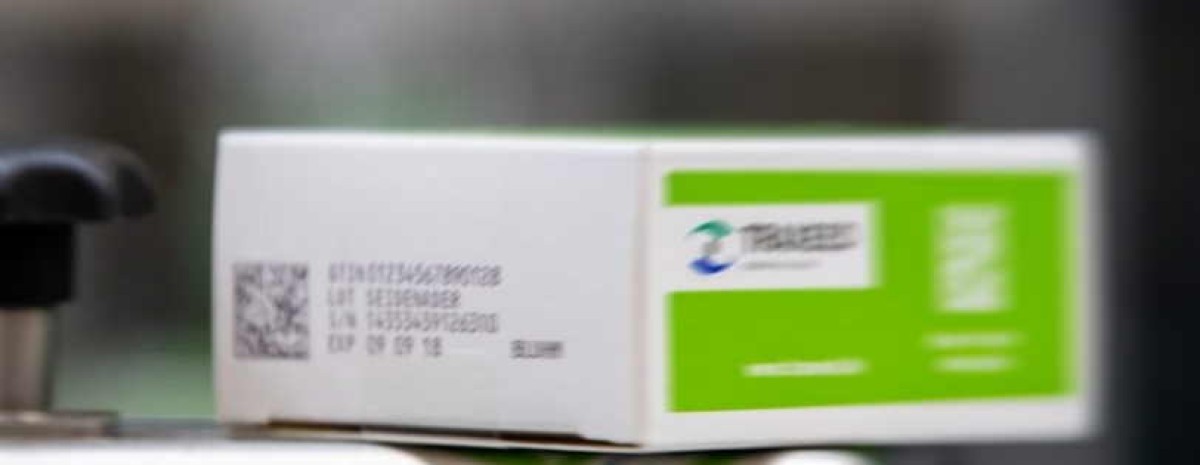
Sono disponibili le istruzioni operative per l’adempimento dei nuovi obblighi per l’implementazione del nuovo sistema anticontraffazione dei medicinali (Dlgs. N.10 6 febbraio 2025) che riguardano l’apposizione sull’imballaggio dei farmaci di un identificativo univoco (UI) codificato in un codice a barre bidimensionale (Data Matrix) e di un sistema di prevenzione delle manomissioni (ATD). Le ha pubblicate l’Aifa come allegato alla Determinazione n.56 del 17 luglio 2025 e derivano direttamente dai due decreti del Ministero della Salute già pubblicati in Gazzetta Ufficiale: quello del 10 aprile 2025, n. 84, che disciplina le specifiche tecniche dell’identificativo univoco, e quello del 9 luglio 2025, che definisce le caratteristiche tecniche e grafiche dei dispositivi di sicurezza. Le nuove norme si applicano a partire dal 9 febbraio 2025, ma sono previsti periodi transitori per l’adattamento graduale del sistema, anche attraverso l’utilizzo del bollino farmaceutico in funzione sostitutiva.
Va precisato che il documento dell’Aifa si rivolge principalmente ai titolari e ai richiedenti di autorizzazioni all’immissione in commercio (AIC) e di autorizzazioni all’importazione parallela (AIP) con specifiche su modalità e tempi per l’inserimento del nuovo bollino sulle confezioni.
L’applicazione delle nuove regole è inquadrata da un periodo di stabilizzazione di due anni, che va dal 9 febbraio 2025 all’8 febbraio 2027. In questa finestra temporale è consentito continuare a utilizzare il bollino farmaceutico in alternativa al sistema completo previsto dal regolamento europeo. L’identificativo univoco (UI) e il sistema anti-manomissione (ATD) possono infatti essere temporaneamente sostituiti dal bollino farmaceutico, che assolve anche la funzione di ATD per qualsiasi medicinale ad uso umano.
In pratica, i medicinali soggetti all’obbligo di UI, destinati al mercato italiano e il cui lotto è stato rilasciato entro il 9 febbraio 2025, possono essere distribuiti e dispensati fino alla loro scadenza, anche se dotati solo del bollino farmaceutico. Lo stesso vale per i lotti rilasciati entro l’8 febbraio 2027, purché recanti il bollino. Durante questo periodo, non è richiesto il riconfezionamento o la rietichettatura di confezioni già stampate.
Parallelamente, Aifa raccomanda che l’aggiornamento delle etichette al template QRD (Quality Review of Documents), modello standardizzato dell’Ema per etichette, Rcp e foglietto che include i nuovi elementi, venga effettuato il prima possibile e in ogni caso entro i termini previsti dal decreto legislativo.
Il cuore del nuovo sistema è l’identificativo univoco (UI), previsto dal regolamento delegato (UE) 2016/161. Si tratta di un codice generato per ogni singola confezione e stampato in formato Data Matrix, che consente la tracciabilità del prodotto lungo tutta la filiera distributiva. Il codice contiene almeno il numero di identificazione del prodotto (il codice nazionale), il numero di serie, la data di scadenza e il numero di lotto. Il tutto è integrato da un elemento di verifica elettronico che abilita l’autenticazione del farmaco tramite appositi sistemi informatici, come previsto anche a livello europeo.
Data Matrix farmaci: cosa legge il farmacista e il lettore ottico. Ecco gli elementi del nuovo codice
A questo si affianca il sistema di prevenzione delle manomissioni (ATD), che riguarda la confezione del medicinale e ha la funzione di segnalare eventuali aperture non autorizzate. Per i medicinali soggetti a UI, l’ATD è rafforzato da un dispositivo apposto sulla confezione che assume la forma di una carta valori, un supporto stampato con caratteristiche tecniche e grafiche stabilite da un apposito decreto interministeriale. Il dispositivo è concepito per resistere a tentativi di contraffazione e può assumere anche una forma digitale, se prevista dal Ministero dell’Economia e delle Finanze.
Non tutti i medicinali sono però soggetti all’obbligo dell’UI. I prodotti esclusi — individuati nell’allegato I del regolamento UE — continueranno a recare il tradizionale bollino farmaceutico come previsto dall’art. 5-bis del d.lgs. 30 dicembre 1992, n. 540, a meno di future modifiche regolatorie.
Anticontraffazione farmaci: in vigore le indicazioni sulle caratteristiche tecniche del nuovo dispositivo di sicurezza
La transizione graduale — attraverso il riconoscimento del valore del bollino farmaceutico nei due anni di stabilizzazione — rappresenta una misura di equilibrio per consentire al sistema industriale e distributivo di adeguarsi senza interruzioni. Al tempo stesso, l’Aifa sottolinea la necessità di pianificare per tempo l’adeguamento degli stampati e delle etichette, in modo da garantire la piena conformità alla nuova disciplina a partire dal 2027.
Fonte
https://www.aifa.gov.it/documents/20142/1099847/All-1_alla%20Determina%20_DTS-56-2025.pdf
https://www.aifa.gov.it/documents/20142/1099847/Determina-DTS%2056-2025_Istruzioni_applicative.pdf
Se l'articolo ti è piaciuto rimani in contatto con noi sui nostri canali social seguendoci su:
Oppure rimani sempre aggiornato in ambito farmaceutico iscrivendoti alla nostra newsletter!
POTREBBERO INTERESSARTI ANCHE
08/04/2026
Pubblicati i regolamenti dei due nuovi strumenti di confronto con pazienti, istituzioni e operatori del settore. Prevista la creazione di un Registro di trasparenza con informazioni sugli incontri...
A cura di Redazione Farmacista33
07/04/2026
Per contrastare l’antibiotico-resistenza servono studi clinici più snelli, sostegno all’innovazione e modelli economici sostenibili per lo sviluppo di nuovi antibiotici. L’Ema punta su scienza...
A cura di Redazione Farmacista33
02/04/2026
La delegazione Aifa guidata dal presidente Robert Nisticò ha incontrato il Ministero della Salute giapponese e l’agenzia regolatoria Pharmaceuticals and Medical Devices Agency per confrontarsi su...
A cura di Redazione Farmacista33
30/03/2026
Dopo una fase pilota di due anni, l’Agenzia europea del farmaco introduce nuove modalità di dialogo scientifico per accelerare lo sviluppo e le preparazioni delle domande di autorizzazione.
A cura di Cristoforo Zervos

©2026 Edra S.p.a | www.edraspa.it | P.iva 08056040960 | Tel. 02/881841 | Sede legale: Viale Enrico Forlanini 21 - 20134 Milano (Italy)